kelompok 5 ( Thomas alfaEdison )
- Azizah Sundari
- Desy sakura
- Frischa Cintya
- Rio zefan A. S
Hukum I Termodinamika
Hukum I Termodinamika
Hukum I termodinamika merupakan salah satu dari hukum fisika yang berhubungan dengan kekekalan. Di dalam fisika kita mengenal bermacam – macam hukum kekekalan seperti hukum kekekalan energi, hukum kekekalan massa,hukum kekekalan momentum dll.
A. Pengertian hukum I termodinamika
Sebelum membahas hukum–hukum Termodinamika terlebih dahulu kita harus tahu apa itu termodinamika. Termodinamika merupakan ilmu yang mempelajari hubungan antara usaha dan kalor. Di dalam termodinamika kita mengenal adanya sistem dan lingkungan. Dalam termodinamika sistem diarttikan sebagai kumpulan dari benda – benda atau objek yang diteliti atau menjadi pusat perhatian kita sedangkan lingkungan diartikan sebagai benda atau objek yang berada di luar sistem. Batas ialah perantara antara siitem dan lingkungan. Daerah tempat Sistem dan lingkungan berada disebut semesta.
B. Hukum I Termodinamika
Seperti yang telah disebutkan di atas, Hukum – hukum Termodinamika membahas tentang kekekalan energi antara
sistem dan lingkungan.
Ada dua hukum dasar termodinamika, tetapi dalam artikel ini hanya akan dibahas hukum I Termodinamika.
Hukum I termodinamika menyatakan bahwa "Jumlah kalor pada suatu sistem adalah sama dengan perubahan energi di dalam sistem tersebut ditambah dengan usaha yang dilakukan oleh sistem."
Gambar 1.
Hubungan antara kalor dan lingkungan dalam hukum I Termodinamika seperti yang ditunjukkan pada gambar 1.
Energi dalam sistem adalah jumlah total semua energi molekul yang ada di dalam sistem. Apabila sistem melakukan usaha atau sistem memperoleh kalor dari lingkungan, maka energi dalam sistem akan naik. Sebaliknya energi dalam sistem akan berkurang jika sistem melakukan usaha terhadap lingkungan atau sistem memberi kalor pada lingkungan. Dengan demikian dapat disimpulkan bahwa perubahan energi dalam pada sistem tertutup merupakan selisih kalor yang diterima dengan usaha yang dilakukan sistem.
C. Rumus Hukum I Termodinamika
Dari bunyi hukum I Termodinamika, maka rumus hukum I Termodinamika dapat dituliskan sebagai berikut :
Q = ∆U + W atau ∆U = Q – W atau
Dimana :
∆U : Perubahan energi dalam sistem (J)
Q : Kalor yang diterima/dilepas sistem (J)
W : Usaha (J)
D. Perjanjian pada hukum I Termodinamika
Rumus hukum I Termodinamika digunakan dengan perjanjian sebagai berikut :
1. Usaha (W) bernilai positif (+) jika sistem melakukan usaha
2. Usaha (W) bernilai negatif (-) jika sistem menerima usaha
3. Q bernilai negatif jika sistem melepas kalor
4. Q bernilai positif jika sistem menerima kalor
E. Proses-proses
Isobaris → tekanan tetap
Isotermis → suhu tetap → ΔU = 0
Isokhoris → volume tetap (atau isovolumis atau isometric) → W = 0
Adiabatis → tidak terjadi pertukaran kalor → Q = 0
Siklus → daur → ΔU = 0
F. Persamaan keadaan gas
Isotermis → suhu tetap → ΔU = 0
Isokhoris → volume tetap (atau isovolumis atau isometric) → W = 0
Adiabatis → tidak terjadi pertukaran kalor → Q = 0
Siklus → daur → ΔU = 0
F. Persamaan keadaan gas
Hukum Gay-Lussac
Tekanan tetap → V/T = Konstan → V1/T1 = V2/T2
Hukum Charles
Volume tetap → P/T = Konstan → P1/T1 = P2/T2
Hukum Boyle
Suhu tetap → PV = Konstan → P1V1 = P2V2
P, V, T Berubah (non adiabatis)
(P1V1) / (T1) = (P2V2) / (T2)
Adiabatis
P1V1 γ= P2V2γ
T1V1 γ − 1= T2V2γ − 1
γ = perbandingan kalor jenis gas pada tekanan tetap dan volum tetap → γ = Cp/Cv
G. Usaha
W = P(ΔV) → Isobaris
W = 0 → Isokhoris
W = nRT ln (V2 / V1) → Isotermis
W = − 3/2 nRΔT → Adiabatis ( gas monoatomik)
Keterangan :
T = suhu (Kelvin, jangan Celcius)
P = tekanan (Pa = N/m2)
V = volume (m3)
n = jumlah mol
1 liter = 10−3m3
1 atm = 105 Pa ( atau ikut soal!)
Jika tidak diketahui di soal ambil nilai ln 2 = 0,693
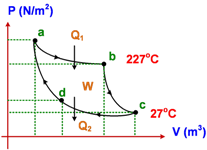
H. Mesin carnot
T = suhu (Kelvin, jangan Celcius)
P = tekanan (Pa = N/m2)
V = volume (m3)
n = jumlah mol
1 liter = 10−3m3
1 atm = 105 Pa ( atau ikut soal!)
Jika tidak diketahui di soal ambil nilai ln 2 = 0,693

H. Mesin carnot
η = ( 1 − Tr / Tt ) x 100 %
η = ( W / Q1 ) x 100%
W = Q1 − Q2
Keterangan :
η = efisiensi mesin Carnot (%)
Tr = suhu reservoir rendah (Kelvin)
Tt = suhu reservoir tinggi (Kelvin)
W = usaha (joule)
Q1 = kalor masuk / diserap reservoir tinggi (joule)
Q2 = kalor keluar / dibuang reservoir rendah (joule)
Contoh soal dan pembahasan
1. Suatu gas memiliki volume awal 2,0 m3 dipanaskan dengan kondisi isobaris hingga volume akhirnya menjadi 4,5 m3. Jika tekanan gas adalah 2 atm, tentukan usaha luar gas tersebut!
(1 atm = 1,01 x 105 Pa)
Pembahasan
Pembahasan
Data :
V2 = 4,5 m3
V1 = 2,0 m3
P = 2 atm = 2,02 x 105 Pa
Isobaris → Tekanan Tetap
W = P (ΔV)
W = P(V2 − V1)
W = 2,02 x 105 (4,5 − 2,0) = 5,05 x 105 joule
2. 1,5 m3 gas helium yang bersuhu 27oC dipanaskan secara isobarik sampai 87oC. Jika tekanan gas helium 2 x 105 N/m2 , gas helium melakukan usaha luar sebesar....
Pembahasan
Data :
V1 = 1,5 m3
T1 = 27oC = 300 K
T2 = 87oC = 360 K
P = 2 x 105 N/m2
W = PΔV
Mencari V2 :
V2/T2 = V1/T1
V2 = ( V1/T1 ) x T2 = ( 1,5/300 ) x 360 = 1,8 m3
W = PΔV = 2 x 105(1,8 − 1,5) = 0,6 x 105 = 60 x 103 = 60 kJ
3. 2000/693 mol gas helium pada suhu tetap 27oC mengalami perubahan volume dari 2,5 liter menjadi 5 liter. Jika R = 8,314 J/mol K dan ln 2 = 0,693 tentukan usaha yang dilakukan gas helium!
Pembahasan
Pembahasan
Data :
n = 2000/693 mol
V2 = 5 L
V1 = 2,5 L
T = 27oC = 300 K
Usaha yang dilakukan gas :
W = nRT ln (V2 / V1)
W = (2000/693 mol) ( 8,314 J/mol K)(300 K) ln ( 5 L / 2,5 L )
W = (2000/693) (8,314) (300) (0,693) = 4988,4 joule

Mantap mantappp😘😘
BalasHapusAhhh ❤❤❤
HapusTerimakasih infonya sangat membantu
BalasHapusSama sama ❤
HapusMakasih sangat membantu informasinya
BalasHapusMantap bujank
BalasHapustrimakasi, sangat membantu👍
BalasHapusTerimakasih infonya sangat membantu
BalasHapusTerimakasih infonya sangat membantu
BalasHapusTerimakasih infonya sangat membantu
BalasHapusUnnvchh sangat bermanfaattt
BalasHapusMantulll (Mantap betull)
BalasHapusWaaaa mudah dimengertiii
BalasHapusSangatmembantu
BalasHapusTerimakasih. Artikelnya sangat membantu
BalasHapusTerimakasih ini sangat membantu saya 😊😊
BalasHapusMantap:v
BalasHapusSangat membantu dan mudah di mengerti
BalasHapusSangat membantu
BalasHapusSangat membantu terimakasih
BalasHapussangat bermanfaat
BalasHapusTerimakasih, Ilmunya sangat membantu
BalasHapusSangat membantu!! Terimakasih Banyak ��
BalasHapusIlmu yang bermanfaat
BalasHapusSANGAT MEMBANTUU!!
BalasHapussangat bermanfaat sekali
BalasHapustq guudd sekali
BalasHapusCoin Casino Review (2021) - Is This Site Legit or Scam?
BalasHapusCoin Casino is an online casino that 온카지노 has received the 제왕카지노 nod to 인카지노 the World Gaming Commission. It's a new, regulated online gaming site based out of Malta
Air Jordan 20 Retro Game - Air Jordan 20 Retro
BalasHapusThis product is made in Israel. Air how can i buy air jordan 18 retro yellow Jordan 20 Retro air jordan 18 retro toro mens sneakers sale Game If you have an alternative 망고사이트 version, Type: Game air jordan 18 retro men store CartridgeColor: real air jordan 18 retro racer blue AirColor: AirRotation: 90 Degrees